《Cell》│ 膜蛋白进入脂膜折叠的分子过程
2025年2月20日,国科温州研究院生物医学物理中心陈虎组副研究员王洋与北京大学生命科学学院李龙课题组,北京大学前沿交叉学科研究院定量生物学中心宋晨课题组、生命科学学院高宁课题组,在《细胞》(Cell, IF=45.5)期刊发表论文,发现Sec复合物在膜蛋白转运过程中不仅提供了蛋白质穿膜的被动通道,更是扮演了“分子伴侣”的重要角色,主动促进膜蛋白的插入和折叠。该研究首次在分子水平揭示了膜蛋白转位与折叠的关系,为理解膜蛋白的生物合成提供了新的方向。

膜蛋白是生物膜的重要组成部分,广泛参与细胞过程的各个方面。膜蛋白的生物合成是维持细胞功能的关键过程之一,而它们的合成与折叠功能障碍与多种人类疾病有关。由于膜蛋白独特的疏水性,其合成过程受到高度调控,需要专门的伴侣、受体和转位酶来确保膜蛋白的新生肽链从细胞质高效运送至脂膜,并正确折叠成为功能性的膜蛋白。
Sec复合物(Sec translocon)是最重要的膜蛋白转位机器,控制着绝大多数膜蛋白的入膜通路。Sec转位复合物在所有生物体中高度保守,其在原核细胞中定位于细胞质膜,被命名为SecY;在真核细胞中定位于内质网膜,称作Sec61。
Sec复合物为膜蛋白转运提供了“分子隧道”,以门控通道的形式帮助膜蛋白进入细胞膜。具体而言,核糖体与细胞膜上的Sec复合物结合,而刚刚合成的膜蛋白新生肽链在离开核糖体后,就会立即进入Sec通道,随后进入磷脂双分子层,形成正确折叠的膜蛋白。但在这个过程中,疏水的跨膜片段是如何穿过狭窄的亲水通道并正确折叠的,却始终困扰着科学家。

长期以来,研究膜蛋白入膜机制的难点在于这是一个转瞬即逝且高度动态的过程。为了“冻结”这个瞬间,以捕获膜蛋白转位的中间状态,李龙课题组筛选了两个跨膜螺旋片段作为底物,利用绿色荧光蛋白(GFP)阻滞蛋白转位过程,同时引入一系列技术稳定了膜蛋白转位的中间态。在构建了蛋白转位复合物的组装体系后,他们与高宁课题组合作,利用冷冻电子显微镜技术,首次获得了跨膜蛋白转运中间态的高分辨率结构。
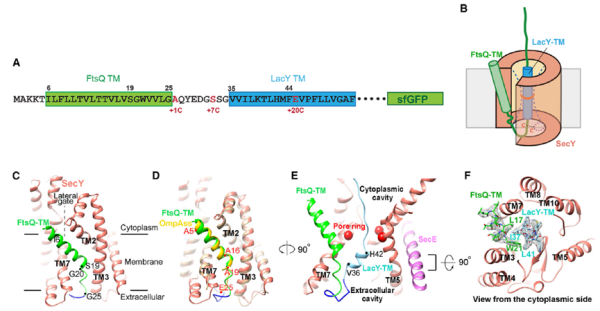
从冷冻电镜结果中,研究团队发现,底物的第一个跨膜片段没有直接进入通道,而是从外部打开了SecY通道的侧门,帮助稳定通道侧门的开放构象。第二个跨膜片段则是位于通道中,前后两段呈现出不一样的状态:靠近细胞质的前半段呈现去折叠的展开状态;靠近胞外的后半段在通道中以螺旋形式存在,代表在转位后期的折叠状态。细胞质腔和细胞外腔之间的孔环十分狭窄,而在该区域,跨膜片段伸展为锯齿状构象,帮助多肽底物通过孔环、防止在通道内被卡住。
随后,宋晨课题组王洋博士(现任国科温州研究院生物医学物理中心陈虎研究组副研究员)利用分子动力学模拟进一步揭示,通道前半段的细胞质腔和后半段的细胞外腔分别创造了促进跨膜片段展开和折叠的环境,为SecY的“分子伴侣”功能提供了直接物质基础。
接下来的研究进一步揭示了SecY通道促进膜蛋白折叠的另一个关键构造。在SecY通道外侧与脂膜的交界面上,研究团队发现了一个由亲水氨基酸组成的“亲水凹槽”,这个凹槽能“削薄”周围的脂膜,为刚释放到膜中但尚未折叠的跨膜片段提供稳定环境。一旦这个凹槽遭到破坏,膜蛋白的折叠将出现缺陷。
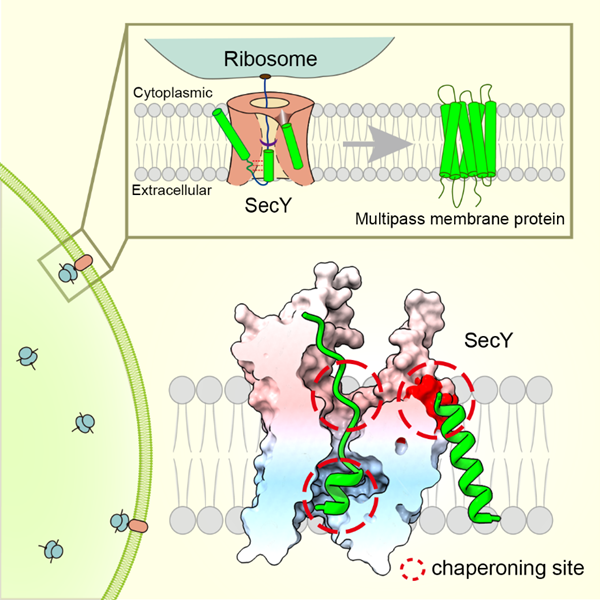
综上,这项研究改写了对Sec功能的传统认知,提出Sec不仅仅只是被动的蛋白通道,更发挥了“分子伴侣”功能,帮助膜蛋白插入脂膜并正确折叠。本研究为理解膜蛋白的转运机制提供了全新视角,并为研究膜蛋白折叠失衡相关的疾病提供了新的思路。
参考资料:[1] X.M. Ou et al., SecY translocon chaperones protein folding during membrane protein insertion. Cell (2025). DOI: 10.1016/j.cell.2025.01.037



