抑制非肌肉肌球蛋白II活性可增强T细胞肿瘤杀伤效能
肿瘤免疫疗法从根本上重塑了肿瘤治疗的格局,而T细胞是肿瘤免疫治疗中的关键细胞,因此在治疗过程确保T细胞的免疫活性成为成功治疗的关键之一。
越来越多的研究表明,机械力学因素和生化因素一样影响T细胞的免疫活性。我院生物力医学与力材料学转化团队在前期的工作中发现,机械力敏感通道PIEZO1可以作为“生物力学免疫检查点”调控T细胞抗肿瘤免疫功能,阻断PIEZO1会增强T细胞肿瘤杀伤效能(Nature Biomedical Engineering 2024, 8:1162-1176)。然而,机械力-生化信号转导通路上其他分子是否也参与T细胞抗肿瘤免疫功能调控,仍然不清楚。
近日,我院生物力医学与力材料学转化熊春阳研究员团队联合中国医学科学院基础医学研究所刘玉英研究员团队在Science Advances发表了题为“Suppression of non-muscle myosin II boosts T cell cytotoxicity against tumors”的论文,发现抑制非肌肉肌球蛋白II(NM II)增加了T细胞的牵引力,进而增强了其对肿瘤细胞的细胞毒性,进一步解析了生物力学因素如何影响T细胞肿瘤杀伤效能。
通过使用来自小鼠和不同类型肿瘤患者的T细胞,研究团队发现低剂量非肌肉肌球蛋白II的抑制剂Blebbistatin可以增强T细胞对肿瘤细胞的细胞毒性,且不影响细胞因子的分泌以及颗粒酶B、穿孔素的产生;部分抑制非肌肉肌球蛋白II活性增强了CD8+ T细胞的牵引力(牵引力显微镜测量结果),也提高了T细胞与肿瘤细胞间的粘附力(流体力显微镜测量结果),提示非肌肉肌球蛋白II参与调控T细胞肿瘤杀伤效能(图1)。
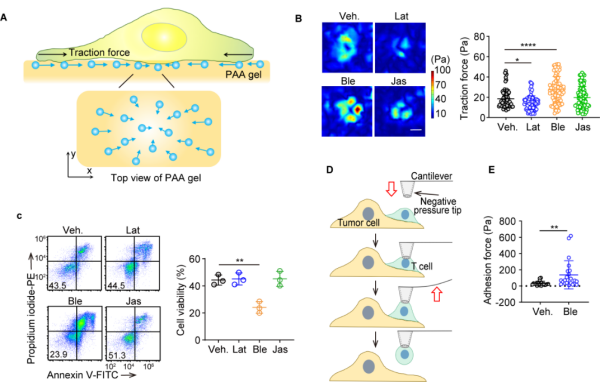
图1. 抑制NM II增强T细胞牵引力及肿瘤杀伤效能。a) T细胞牵引力检测示意图;b) 小分子药物抑制NM II增强T细胞牵引力;c)小分子药物抑制NM II增强T细胞的肿瘤杀伤效果;d)流体力显微镜检测T细胞与肿瘤细胞间粘附力;e)小分子药物抑制NM II增强T细胞与肿瘤细胞间粘附。
进一步探究其机理发现:非肌肉肌球蛋白II上调转录因子NKX3-2活性,进而增加其靶基因ADGRB3表达;而ADGRB3上调则抑制丝状肌动蛋白(F-actin)动态重塑,导致T细胞牵引力下降,最终减弱了T细胞肿瘤杀伤功能(图2)。在动物肿瘤模型中,靶向T细胞NMII-NKX3-2-ADGRB3通路能有效抑制肿瘤生长,延长生存期。在结直肠癌、胃癌和肝癌等肿瘤病人样本中,也发现NKX3-2、ADGRB3表达水平与患者CD8+T细胞的浸润程度、免疫治疗效果负相关。
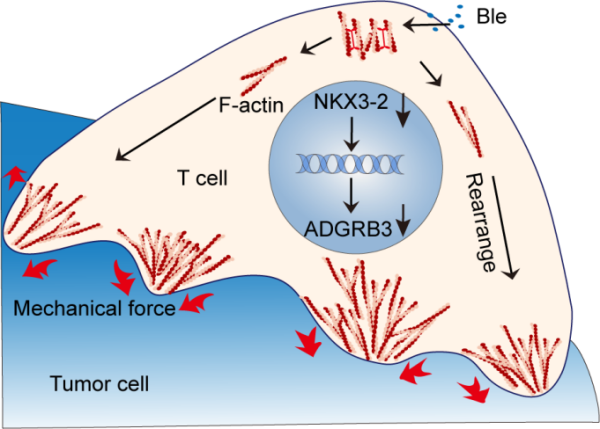
图2. NMII-NKX3-2-ADGRB3信号通路调控T细胞肿瘤杀伤的力学生物学机制示意
该研究为机械力信号调控T细胞抗肿瘤免疫功能提供了新的证据,也为研发更有效的肿瘤免疫疗法提供了生物力学新策略。
我院生物力医学与力材料学转化团队林峰副研究员、北京协和医院杨莹韵副主任医师、中国医学科学院基础医学研究所博士生温达瀚为论文的共同第一作者。熊春阳教授和刘玉英研究员、李开龙教授为该论文的共同通讯作者。



