通过不同构象之间转换的非平衡稳态动力学理论研究人葡萄糖激酶合作效应的最优条件
2021-05-14 15:41:00
近日,牟维华副研究员与美国麻省理工学院的Jianshu Cao教授和Jing Kong教授合作,完成了一项酶动力学方面的理论研究,解释了最近Miller及其合作者报道的与人葡萄糖激酶合作效应有关的现象。
人葡萄糖激酶催化葡萄糖底物,得到产物6-磷酸葡萄糖。这个酶对维持体内平衡起着重要的作用。 Miller及其合作者发现当人葡萄糖激酶的两个特征速率常数接近时,酶合作效应比较显著。人葡萄糖激酶只有一个与底物结合的位点,所以它的合作效应不是异构作用的结果,应是一种动力学效应,来自于酶的非平衡构象涨落,这是一个有意义的理论问题。鉴于人葡萄糖激酶的生理作用,用物理化学理论去分析解释它的动力学合作现象,有助于人们理解这类酶的作用机理及研究可能的调控手段。
根据Miller及合作者通过实验总结出来的人葡萄糖激酶的反应网络,牟维华副研究员和合作者们考虑了酶在反应过程中的构象变化,研究了不同构象之间转换的非平衡过程,发展了单体酶的动力学合作效应理论,给出了这类酶的反应进行曲线的一般表达式,特别是合作效应的显示表达式,论证了在生理条件下,人葡萄糖激酶的特征速率常数和合作效应之间的关系,从而解释了Miller及其合作者观察到的合作效应随特征速率常数变化的动力学“共振”现象。牟维华副研究员和合作者们在这一工作中所发展的理论方法可用于研究与酶构象变化有关的其他生物学现象。
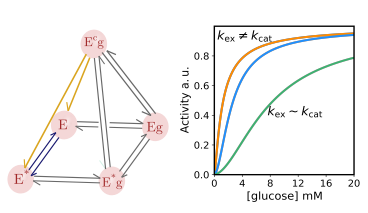 该工作于2021年3月16日在线发表于The Journal of Physical Chemistry Letters期刊 (IF: 6.71) 。
该工作于2021年3月16日在线发表于The Journal of Physical Chemistry Letters期刊 (IF: 6.71) 。
人葡萄糖激酶催化葡萄糖底物,得到产物6-磷酸葡萄糖。这个酶对维持体内平衡起着重要的作用。 Miller及其合作者发现当人葡萄糖激酶的两个特征速率常数接近时,酶合作效应比较显著。人葡萄糖激酶只有一个与底物结合的位点,所以它的合作效应不是异构作用的结果,应是一种动力学效应,来自于酶的非平衡构象涨落,这是一个有意义的理论问题。鉴于人葡萄糖激酶的生理作用,用物理化学理论去分析解释它的动力学合作现象,有助于人们理解这类酶的作用机理及研究可能的调控手段。
根据Miller及合作者通过实验总结出来的人葡萄糖激酶的反应网络,牟维华副研究员和合作者们考虑了酶在反应过程中的构象变化,研究了不同构象之间转换的非平衡过程,发展了单体酶的动力学合作效应理论,给出了这类酶的反应进行曲线的一般表达式,特别是合作效应的显示表达式,论证了在生理条件下,人葡萄糖激酶的特征速率常数和合作效应之间的关系,从而解释了Miller及其合作者观察到的合作效应随特征速率常数变化的动力学“共振”现象。牟维华副研究员和合作者们在这一工作中所发展的理论方法可用于研究与酶构象变化有关的其他生物学现象。

Weihua Mu, Jing Kong, and Jianshu Cao, "Understanding the Optimal Cooperativity of Human Glucokinase: Kinetic Resonance in Nonequilibrium Conformational Fluctuations", J. Phys. Chem. Lett. 2021, 12, 2900-2904.
论文链接: https://pubs.acs.org/doi/10.1021/acs.jpclett.1c00438


